In a recent study, pulses of the sugar glucose restoreed normal insulin release in pancreas cells, which could shed light on loss of insulin release in Type 2 diabetes.
Pulses of the sugar glucose can restore normal insulin release in mouse pancreas cells that have been exposed to excess glucose, according to a study published in PLOS Computational Biology.
This finding could improve understanding of high blood sugar, also known as hyperglycemia, which is a hallmark of Type 2 diabetes.
In a healthy person, pancreas cells known as beta cells regulate blood sugar by releasing pulses of insulin into the bloodstream. These pulses curb glucose output from the liver and prompt tissues throughout the body to absorb glucose.
In a person with hyperglycemia, however, exposure to excess glucose deactivates the beta cell “clock” that sets the rhythm of insulin pulses, and not enough insulin is produced.
Continue Reading Below ↓↓↓
In the new study, Joseph McKenna and colleagues from Florida State University developed a mathematical model that suggests pulses of glucose could potentially restart the insulin clock in beta cells that have been exposed to excess glucose.
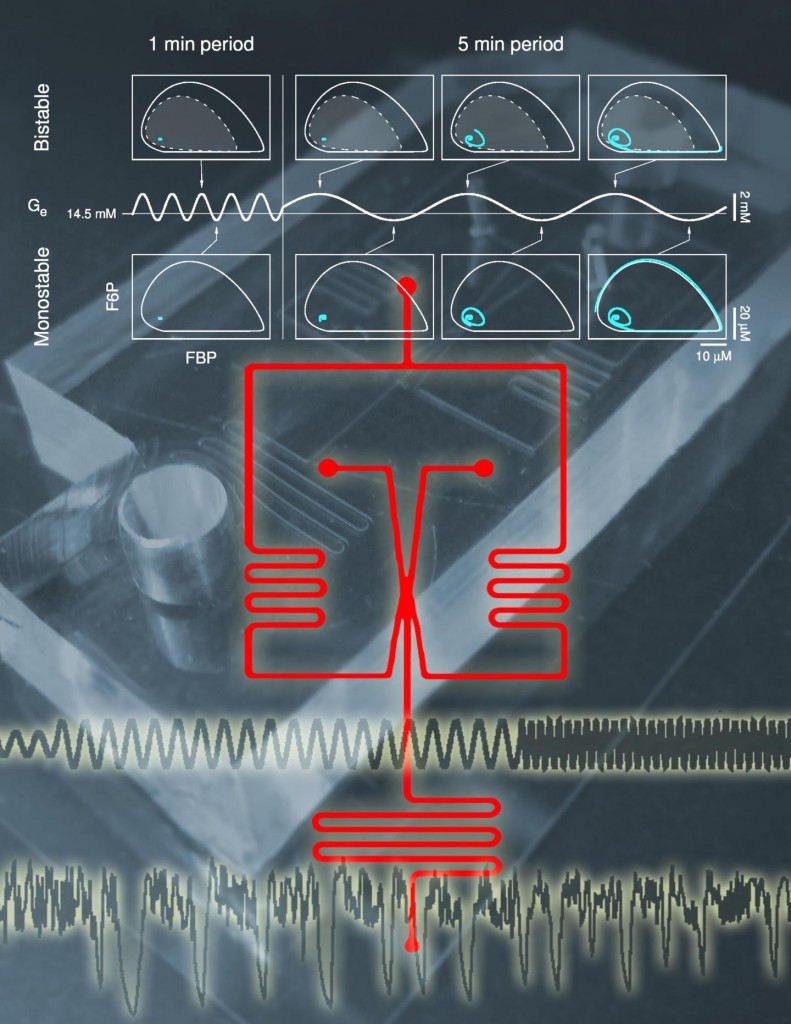
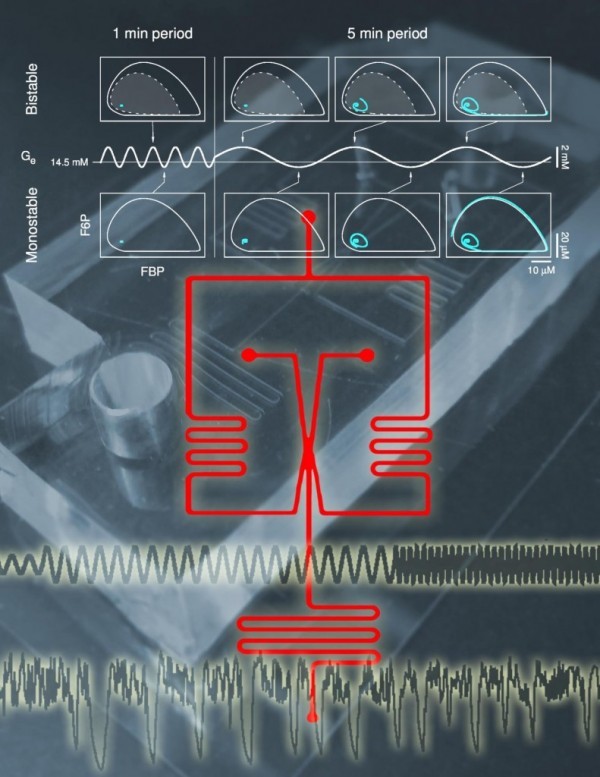
To put this prediction to the test, they removed groups of beta cells, called islets of Langerhans, from non-diabetic mice and placed them in a small chamber. A specially engineered device then exposed the islets to controlled microfluidic flows of a glucose solution.
The researchers found that high, steady glucose concentrations deactivated the beta cell insulin clock in the mouse islets. However, controlled pulses of glucose reactivated the clock. The scientists also found that reactivated islets could recruit and reactivate other islets when the glucose solution flow was controlled by a feedback loop that mimics the action of the liver.
“This article demonstrates how microfluidics and mathematical modeling can be used together to gain new insights into the mechanisms for hormone secretion,” says study co-author Richard Bertram.
Future research will use similar techniques to study islets from diabetic mice, as well as islets from both diabetic and non-diabetic people.
Related PLOS Computational Biology Article: Glucose Oscillations Can Activate an Endogenous Oscillator in Pancreatic Islets
Citation: McKenna JP, Dhumpa R, Mukhitov N, Roper MG, Bertram R (2016) Glucose Oscillations Can Activate an Endogenous Oscillator in Pancreatic Islets. PLoS Comput Biol 12(10): e1005143. doi:10.1371/journal.pcbi.1005143
Source: PLOS
Journal: PLOS Computational Biology
Photo credit: Bertram et al.
Funding: This research was supported by grant number DK080714 to RB and MGR from the National Institutes of Health. The funders had no role in study design, data collection and analysis, decision to publish, or preparation of the manuscript.
Competing Interests: The authors have declared that no competing interests exist.